色水法在商业化生产中的应用(激光打孔 玻璃微滴管)CCIT发表时间:2021-02-05 10:39 01 法规对商业化生产密封性的要求 药品包装密封性质量控制的重要一环是商业化生产中药品的密封性,依据《化学药品注射剂包装系统密封性研究技术指南(试行)》,需“基于风险评估,以及产品开发、验证、生产阶段积累的包装密封性数据,开展商业化生产密封性检查。熔封的产品(如玻璃或塑料安瓿等)应当作100%的密封性检测,其他包装容器的密封性应当根据操作规程进行抽样检查。对于大容量软袋包装等风险较高的产品,建议在工艺验证中增加一定样品量的密封性检查,确认拟定的包装材料、生产工艺的可行性;在商业化生产中科学制定取样计划,增加取样数量和频次;具备条件的进行100%密封性检查”。 从指南的上述描述不难看出,针对化药注射剂商业化生产阶段的密封性要求,可以依据包装形式分成三类:
第一类为安瓿,包括玻璃安瓿和塑料安瓿,密封机制本身存在一定泄漏的可能性,需要进行100%检测; 第二类为大容量软袋,其泄漏风险也比较高,需增大抽样量,有条件的企业可以进行100%密封性检查; 第三类为除了上述包装形式之外的其他包装,一般为西林瓶、预灌封、输液瓶等通过物理配合密封(PhysicallyMated Closures),这类包材一般都有胶塞、硅胶垫等弹性体作为辅助密封件,生产工艺可以提供稳定的密封性,只需要进行抽样检查。 对于只需抽样检测的制剂,一般采用经过验证的线下方法即可,常用的线下方法有真空衰减、压力衰减、质量提取、高压放电等,可依据制剂、包材的性质特点选择合适的方法;对于需要100%检测的塑料安瓿和玻璃安瓿,则需要线上设备进行检测。目前线上常用的设备有高压放电法、色水法、激光顶空以及少量企业还在使用的负压检漏。 本文主要介绍色水法在商业化生产中的应用。 02 色水法检漏原理
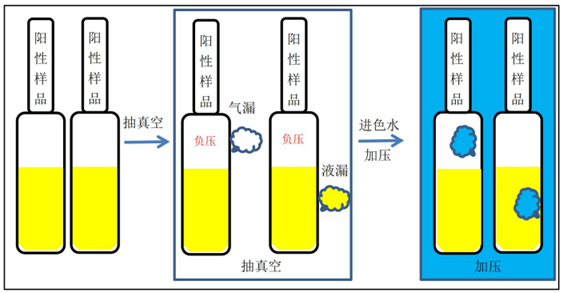
商业化生产的色水法检漏机一般与灭菌柜一体,在灭菌结束后直接进行检漏,其基本原理是通过对样品进行加压减压处理、在样品内外制造压差从而使色水在压差作用下进入样品。一般,在条件比较严苛的条件下,色水法灵敏度(100%检出的孔径)可以达到3µm
03 色水法适应范围 色水法只适合玻璃安瓿的检测,塑料安瓿由于清洗困难,并不适合色水法检漏。无色安瓿和棕色安瓿均可以使用,但棕色安瓿比无色安瓿检测条件要相应的更苛刻一些。另外由于色水法需要灯检,一些需要避光保存的样品无法使用色水法检测。 04 色水法灵敏度的影响因素 色水法作为一种概率性方法,试验过程中的诸多因素都会影响其灵敏度,主要影响因素有: 1. 色水法试验条件:染色剂种类、浓度、真空度/保持时间、压力/保持时间; 2. 制剂的特点包括包材的颜色、制剂的颜色、制剂的规格、制剂的成分、粘稠度等等; 3. 目视法检测人员对颜色的敏感度等主官因素。 这些因素往往并不是独立产生影响,而是需要综合来看,比如染色剂种类,除了要考虑染色剂本身的显色性能、染色液的表明张力、清洗的难易程度,还要考虑染色剂和包材颜色以及制剂性质的相容性,需要选择与制剂具有相容性的染色剂种类。另外,样品规格的影响也是多方面的。
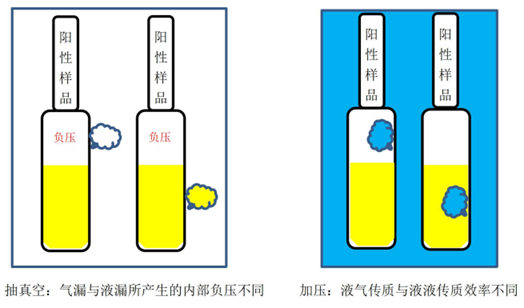
一般情况下,可在线上验证之前,采用线下设备对色水条件进行初步摸索,确定好色水浓度、压力条件和保持时间这些条件,然后进一步将方法转移至线上设备。如果要达到3µm的灵敏度,色水浓度至少需在0.01%以上,当然高的色水浓度也会相应的增加清洗难度。依据现有经验来看,不同染色剂清洗难度并不相同,在方法摸索阶段,针对清洗难度进行染色剂筛选是有必要的。 05 阳性样品打孔位置考虑 每一种检测方法都会涉及打孔位置的考虑,我们在考虑打孔位置的时候,应该秉持“风险评估”的原则,即首先分析制剂本身的泄漏风险,而风险又可以从风险点的位置和风险类型去考虑。对于安瓿来说,主要泄漏风险位置在熔封部位,其次,瓶颈可能存在的一些肉眼不易察觉的裂痕,这两个点的泄漏风险类型均为气漏(色水法检漏一般样品正置,漏点位于制剂液面以上,抽真空时顶空气体从泄漏位点逸出,本文称为气漏)。如果还要更加全面的去关注风险,可以考虑一些风险低的部位,如瓶子底部或者瓶身部位,这些漏点的泄漏类型为液漏。 色水法作为一种整体检漏方法,阳性样品孔径一旦经过计量被确定,其结果只跟泄漏类型有关、与泄漏位置无关,因此,在考虑打孔位置时,可以主要考虑在气漏部位打孔,辅以液漏部位,并不需要非要定点制备在熔封部位和瓶颈,这是整体检漏方法与定点检漏方法的区别。 气漏和液漏阳性样品的检测灵敏度会有一定的差异性,差异性的大小与很多因素有关。一般而言,只要色水浓度、压力条件和保持时间合适,不管是无色安瓿还是棕色安瓿,色水法可以100%检出3µm的泄漏。
06 线上色水检测其他需要考虑的问题 1、环境污染问题 色水法在密封性检测中已经有很长的应用历史,但是由于在相应的法规出台之前,大家往往只关注较大的泄漏,使用的色水浓度都比较低,色水使用后通过污水直接排放。色水法灵敏度提高的关键因素之一是色水浓度,当将色水浓度提高至0.01%甚至更高的情况下,色水的排放变成了一个非常严重的环境污染问题。从笔者接触的一些药企反映,色水很少会进行重复性利用,即便是重复性利用,利用次数也有限,原因之一是色水使用之后浓度往往会被稀释,浓度降低;另外一个重要原因是配制色水的水是一般的纯化水,并没有严格的微生物控制,在放置一段时间之后,水中的微生物增加明显使得色水不具有重复利用的可能。 目前色水法申报的合规性一般通过将其与微生物挑战法关联获得,即要求其灵敏度与微生物挑战法相当或者高于微生物挑战法,而微生物挑战法灵敏度与挑战条件相关,在法规没有对微生物挑战条件进行规定的前提下,色水法的灵敏度要求也变得模糊,而高的灵敏度意味着更高的色水浓度,更多的环境污染。 2、色水检漏引起的染菌风险 色水检漏法另一个需要关注的问题是色水检漏是在灭菌之后进行,虽然整个过程在灭菌柜中进行,但整个色水体系并不是无菌的,配制色水所使用的纯化水并非无菌水,这也意味着色水本身含有微生物,而色水检漏本身有一定的灵敏度,假设检漏灵敏度为5µm,这就意味着低于5µm的漏孔是无法被检出的,而在漏孔高于0.3µm时有通过液体激发微生物进入的风险,如果样品存在低于5µm的漏孔,由于在色水检漏过程中经历了抽真空/加压这些剧烈的条件,是否会因此增加微生物侵入的风险?毕竟一般药品在生命周期中只会接触空气中的微生物,也不会经历这样严苛的条件,由液体激发的微生物侵入风险比较低。 这个问题是由药企的资深人员提出,笔者也配合他们做了相应的研究。我们通过在阳性样品中罐装培养基,将其浸没在纯化水中按照色水法的条件进行抽真空/加压处理,处理之后再进行培养,观察阳性样品染菌情况。试验结果表明在纯化水中微生物含量为50cfu/ml时,3µm、5µm的阳性样品均没有长菌,而10µm的阳性样品有20%的侵入概率。而色水法本身可以将5µm、10µm的泄漏100%检出,综合来看,通过控制纯化水中微生物含量、提高色水检漏的灵敏度,可以控制色水法引起的染菌风险。一般3µm的泄漏在色水法检漏中色水进入的量在5µl-10µl左右(经验值,仅供参考),在纯化水中微生物含量为50cfu/ml时,其侵入量仅为≤0.5 cfu,故其染菌的风险比较低。这也意味着如果染色液重复使用会导致其中微生物含量增加的话,色水检漏引起的微生物进入风险也会相应的增加。 3、色水检漏验证要不要验证灭菌过程? 色水检漏是在灭菌柜中进行的,在灭菌结束之后运行检漏程序,那么使用阳性样品验证检漏过程是不是要经历灭菌过程?这个问题可以从“要验证”与“不需要验证”两个角度去评估验证过程的合理性。 首先,秉持要验证灭菌过程的观念评估的是在灭菌之前样品存在的泄漏,所以认为阳性样品应当和样品一样经历灭菌,这样才能模拟真实情况,但阳性样品经历灭菌过程其孔径会发生变化,这种变化除了与灭菌条件有关,还与制剂的成分、性质有关。粘稠的制剂在灭菌过程容易堵塞漏孔,制剂成分在高温高压条件下对于漏孔的腐蚀也可能导致漏孔堵塞,高温高压环境的变化有可能导致漏孔变大,这诸多因素的影响使得灭菌后阳性样品的孔径变化难以预估,所以,检漏验证容易出现不可预期的结果。 其次,如果不进行灭菌、只进行检漏验证评估的则是在灭菌之后样品存在的泄漏,而这些泄漏也是将来在样品生命周期中存续的泄漏。由于没有上述因素的影响,试验结果会呈现随着孔径增大染色概率逐渐升高的趋势。个人认为检漏验证不进行灭菌更好一些,因为灭菌和检漏是两个完全独立的过程行使的是不同的功能,我们对于检漏的验证是验证仪器检出泄漏的能力,应该排除灭菌过程对于孔径变化的干扰,而我们真正要评估的泄漏风险也是灭菌之后样品可能存在风险,而不是灭菌之前。
|